Általános hírek
SCIP bejelentés
A hulladékokról szóló 2008/98/EK irányelv módosításáról szóló (EU) 2018/851 európai és parlamenti és tanácsi irányelv írja elő 2021. január 5-től a vegyi anyagok regisztrálásáról, értékeléséről, engedélyezéséről és korlátozásáról szóló 1907/2006/EK európai parlamenti és tanácsi rendelet (a továbbiakban: REACH rendelet) 3. cikk 33. pontjában definiált árucikk szállítóinak az ún. különös aggodalomra okot adó anyagoknak (a továbbiakban: SVHC) az Európai Vegyianyag-ügynökség (a továbbiakban: ECHA) számára történő bejelentési kötelezettségét az aggodalomra okot adó anyagokkal kapcsolatos cikkek vagy összetett tárgyak (termékek) információinak adatbázisába (Substances of Concern In articles as such or in complex objects Products – SCIP). Az adatbázis lehetővé teszi, hogy az SVHC anyagokat tartalmazó árucikkekkel kapcsolatos információk rendelkezésre álljanak a termékek és anyagok teljes életciklusa alatt, beleértve a hulladékfázist is.
A kötelezettség szempontjából fontos kiemelni, hogy az összetett (azaz több árucikkből álló) tárgyakban található árucikkekre is vonatkozik a REACH rendelet 33. cikk szerinti kötelezettség mindaddig, amíg az említett „összetevő” árucikkek megtartják különleges formájukat, felületüket vagy alakjukat, ami által a REACH rendelet 3. cikk 3. pontja értelmében árucikknek minősülnek, illetve amíg nem válnak hulladékká. Ennek megfelelően SVHC 0,1 tömegszázalékos koncentrációját minden esetben az érintett (rész)árucikk tömegéhez kell viszonyítani és a kötelezett szereplőknek minden egyes olyan (rész)árucikket be kell jelenteniük, amely ennél nagyobb koncentrációban tartalmaz SVHC-t.
A bejelentésre kötelezettek körét a REACH rendelet 3. cikk 33. pontja és a 31. cikk (1) bekezdése együttesen határozza meg, amely szerint egy árucikk szállítójának az árucikk gyártója vagy importőre, a forgalmazó vagy a szállítói lánc más szereplője minősül, aki az árucikket piaci forgalomba hozza. Ugyanakkor a 33. cikk (1) bekezdése csak azon forgalomba hozatalra vonatkozóan ír elő kötelezettséget, amely a REACH rendelet 3. cikkének 35. pontjában meghatározott ’árucikk átvevő’, azaz ipari vagy foglalkozásszerű felhasználó vagy forgalmazó felé történik.
Ennek megfelelően, a következő árucikk-szállítóknak kell információt szolgáltatniuk az ECHA felé:
- az árucikk uniós előállítói és összeszerelői,
- az árucikk uniós importőrei,
- az árucikk uniós forgalmazói és a szállítói lánc árucikkeket forgalmazó egyéb szereplői, a közvetlenül és kizárólag a fogyasztóknak árucikkeket szállítók kivételével.
Az ECHA-nak való információszolgáltatás kötelezettsége az első szállítótól (előállító/importőr) kezdődik. A REACH rendelet tekintetében az import az Európai Gazdasági Térség tagállamain (EGT: EU-tagállamok, Norvégia, Liechtenstein és Izland) kívüli országból történő behozatalt jelenti.
Az árucikk előállítóira/összeszerelőire és importőreire vonatkozó bejelentési kötelezettség abban az esetben is fennáll, ha kizárólag fogyasztók számára hozzák forgalomba az árucikkeket.
A SCIP adatbázisba történő bejelentési kötelezettség magyar jogrendbe történő átültetése az egyes energetikai és hulladékgazdálkodási tárgyú törvények módosításáról szóló 2021. évi II. törvény révén valósult meg, amely a kémiai biztonságról szóló 2000. évi XXV. törvényt (a továbbiakban: Kbtv.) módosítva ültette át az alábbi, 2021. március 1-től hatályos rendelkezést:
„11.§. A REACH 3. cikk 33. pontjában meghatározott árucikk bármely szállítója a REACH 33. cikk (1) bekezdésének megfelelően az e célból biztosított formátum és benyújtási eszköz felhasználásával tájékoztatja az Európai Vegyianyag-ügynökséget.”
A SCIP adatbázisba történő bejelentéssel kapcsolatban további információ az ECHA weboldalán érhető el.
A kötelezettséggel kapcsolatban a Nemzeti Népegészségügyi Központ (NNK) nem rendelkezik hatáskörrel. Az érdekelt felek a bejelentéssel kapcsolatos részletszabályok vonatkozásában, a kötelezettség végrehajtásának ellenőrzésére – a Kbtv. 32. §. (1) bekezdésének g) alpontja alapján – kijelölt hulladékgazdálkodási hatósághoz fordulhatnak (ld. a 124/2021. (III. 12.) Korm. rendeletet: http://njt.hu/cgi_bin/njt_doc.cgi?docid=248074.421699).

Forrás: ECHA
Bejelentéssel kapcsolatos hírek
Magyarország is fogadja a bejelentéseket a PCN portálon
Több ízben érkezett kérdés az NNK-hoz arra vonatkozóan, hogy Magyarország is fogadja-e már az ECHA méregközponti portálján (PCN) keresztül benyújtott bejelentéseket.
A válasz igen: 2020. december 18-tól Magyarország is fogadja az 1272/2008/EK rendelet (a továbbiakban: CLP rendelet) VIII. melléklete szerinti bejelentéseket a PCN portálon keresztül. Ez azt jelenti, hogy az NNK Kémiai Biztonsági és Kompetens Hatósági Főosztályának (KBKHF) Egészségügyi Toxikológiai Tájékoztató Szolgálat és Bejelentési Osztálya ettől az időponttól ellenőrzi tartalmilag a bejelentéseket.
A bejelentésre kötelezettek nagymértékű aktivitást mutattak és mutatnak jelenleg is az új bejelentéssel kapcsolatban, az alábbi táblázat és diagram – főként – a 2020. évi tendenciát szemlélteti a benyújtott bejelentések tekintetében:
|
Év |
2020 |
2020 |
2020 |
2020 |
2020 |
2020 |
2020 |
2020 |
2020 |
2020 |
2020 |
2021 |
Összesen |
|
Bejelentések |
226 |
370 |
276 |
391 |
527 |
387 |
537 |
853 |
1460 |
4813 |
25586 |
25491 |
60917 |
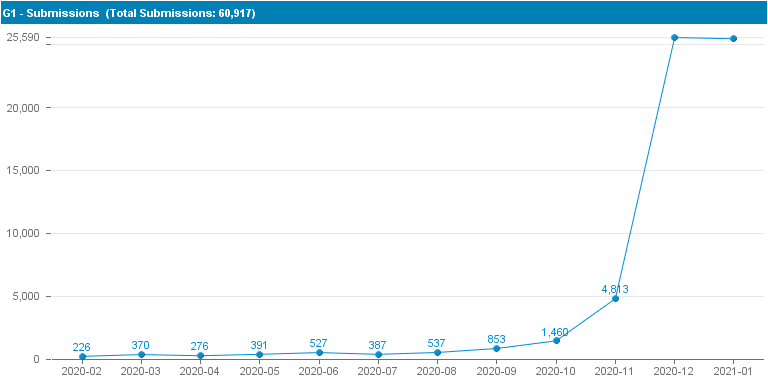
január 1-jétől április közepéig, több mint 49000 db bejelentés került benyújtásra a PCN portálon keresztül KBKHF felé. A bejelentések feldolgozása KBKHF részéről folyamatosan történik.
PCN bejelentések szakmai ellenőrzése
Az NNK Kémiai Biztonsági és Kompetens Hatósági Főosztálya részéről az ECHA PCN bejelentési portálján beérkező veszélyes keverék bejelentések feldolgozása folyamatosan történik.
Az NNK a bejelentéseket szúrópróbaszerűen ellenőrzi (a termék forgalomba hozatala nem függ az NNK jóváhagyásától, a bejelentés benyújtásával a bejelentő eleget tesz a jogszabály által előírt bejelentési kötelezettségének, azaz a termék forgalmazható) és az esetleges hiányosságok feltárása esetén, vagy amennyiben további kiegészítést tart szükségesnek, kéri az adott bejelentés kiegészítését, korrekcióját. A bejelentések fogadásáról a PCN portál által biztosított rendszerinformáción kívül az NNK további, külön tájékoztatást nem küld a bejelentő partnereknek. Fentiekre tekintettel, az NNK akkor veszi fel a kapcsolatot az adott bejelentő céggel, ha kérdés, pontosítás merül fel a bejelentéssel kapcsolatban.
Az ügyintézés megkönnyítése érdekében kérjük a bejelentőket, hogy a bejelentés díjának rendezéséről szóló befizetési igazolást küldjék meg a Ez az e-mail-cím a szpemrobotok elleni védelem alatt áll. Megtekintéséhez engedélyeznie kell a JavaScript használatát. e-mail címre a terméknév és a hozzá tartozó benyújtási szám (submission number), valamint a bejelentés napjának megadásával (lehetőség szerint Excel formátumban). Mindezeken túl, a befizető adószámának megküldése is szükséges.
Az azonosítható befizetést követően a befizető nevére, címére és adószámára kiállított számla a bejelentésben megadott e-mail címre kerül megküldésre. Amennyiben a befizetőnek egy másik, a bejelentés során megjelölttől eltérő e-mail címére kérik a számlát, akkor azt is a fent említett információk megküldésével egyidejűleg jelezzék. Az NNK csak egy, a befizetőhöz tartozó e-mail címre küld számlát. A számla kiállításához szükséges adatok: cég neve, címe, adószáma.
Tevékenység bejelentés a PCN portálon, azaz az új bejelentési kötelezettség téves értelmezése
Több megkeresés érkezett az NNK-hoz arra vonatkozóan, hogy a cégek/vállalkozások a veszélyes anyaggal és keverékkel végzett tevékenységüket az Európai Vegyianyag-ügynökség (ECHA) méregközponti (PCN) portálján keresztül kívánják (vagy már megkísérelték) bejelenteni, amely azonban különböző okokból kifolyólag problémába ütközött, meghiúsult (pl. a tájékoztatással ellentétben nem magyar, hanem angol nyelvű a felület, probléma a regisztráció/belépés során, nincs tájékoztatás a PCN portálon megtett tevékenység bejelentés kivitelezéséről, stb.).
Fontos azonban tisztázni, hogy két, egymástól független, különböző bejelentési kötelezettségről van szó.
1. Európai Vegyianyag-ügynökség (ECHA) méregközponti (PCN) portálján keresztül történő bejelentés:
A CLP rendelet 45. cikke és az (EU) 2017/542 rendelettel elfogadott VIII. melléklete értelmében az egészségre gyakorolt vagy fizikai hatásai alapján veszélyesként osztályozott keveréket forgalomba hozó importőröknek (aki a keveréket az Európai Unióba behozza) és továbbfelhasználóknak (kifejezetten a keverék uniós előállítója) meghatározott információkat kell benyújtaniuk azon tagállamok kijelölt szerveihez, ahol a keveréket forgalomba kívánják hozni. A VIII. melléklet rendelkezéseket állapít meg az egészséget érintő vészhelyzetre való reagálással kapcsolatos azon információk harmonizálására vonatkozóan (mind formailag, mind tartalmilag), amelyeket az uniós piacon veszélyes keverékeket forgalomba hozó vállalatoknak az egyes tagállamok által kijelölt szervekhez (Magyarországon az NNK szervezeti keretein belül működő Egészségügyi Toxikológiai Tájékoztató Szolgálathoz – röviden ETTSZ) be kell nyújtaniuk. Az előírt információk közé tartoznak többek között a következők: a keverék azonosítása (pl. UFI), veszélyeinek megadása, összetétel, felhasználás. A bejelentés célja, hogy a méregközpontok gyorsan azonosítható, pontos információkkal rendelkezzenek egy esetleges mérgezési balesetre vonatkozó tanácsadáskor. Az összetételre vonatkozó részletes információk hiánya pl. akadályozhatja vészhelyzet esetén az orvosi tanácsadást vagy a kockázatkezelési intézkedések hatóságok általi megállapítását. Azokban az esetekben, amikor a toxikológiai központ nem fér hozzá a keverékek teljes összetételéhez, a vészhelyzet esetén tett válaszintézkedés potenciálisan helytelen orvosi tanácsadáshoz és/vagy túlkezeléshez vezethet. Az egyedi formulaazonosító (UFI) lehetővé teszi a toxikológiai központok számára, hogy egyértelműen azonosítsák a keveréket, és mérgezés esetén javaslatot tegyenek a megfelelő orvosi kezelésre. Az információkat elektronikusan, meghatározott formátumban kell benyújtani, amely lehetővé teszi a kijelölt szervek számára, hogy egyszerűen visszakeressék az érintett adatokat. A CLP rendelet szerinti bejelentéseket Magyarország kizárólag az ECHA méregközponti portálján (PCN) keresztül fogadja.
2. Veszélyes anyaggal és keverékkel végzett tevékenység bejelentés:
A tevékenység bejelentés kizárólag a veszélyes anyagokkal és keverékekkel végzett cselekvésre fókuszál (pl. felhasználás, forgalmazás, gyártás, stb.) és a bejelentésre minden esetben magyarországi partner a kötelezett. Minden olyan cégre, vállalkozásra, szolgáltatóra vonatkozik a bejelentési kötelezettség, aki a veszélyes anyagokkal/keverékekkel a kémiai biztonságról szóló 2000. évi XXV. törvény 1. § (2) bekezdés g) pontja szerinti tevékenységet végez. Emiatt a bejelentésben a veszélyes anyagokkal/keverékekkel végzett tevékenységeket kell tételesen bejelölni. A tevékenység bejelentés célja, hogy a hatóság nyilvántartással rendelkezzen az illetékességi területén lévő veszélyes anyagokkal/keverékekkel történő tevékenységekről. A bejelentést a veszélyes anyagokkal és a veszélyes készítményekkel kapcsolatos egyes eljárások, illetve tevékenységek részletes szabályairól szóló 44/2000. (XII. 27.) EüM rendelet 9. § (1) bekezdésében meghatározott módon, azaz az Országos Szakrendszeri Információs Rendszer Kémiai Biztonsági Szakrendszeren (OSZIR-KBIR) keresztül kell megtenni a területileg illetékes kerületi/járási hivatalok népegészségügyi osztálya felé (az illetékes népegészségügyi osztályok elérhetőségei a www.kormanyhivatal.hu weboldalon megtalálhatók). Mindezek alapján látható, hogy a veszélyes anyaggal és keverékkel végzett tevékenység bejelentés rögzítése nem a PCN portálon keresztül történik.
Fentiekből látható továbbá, hogy bár két különböző bejelentési kötelezettségről van szó, adott esetben lehetnek átfedések az érintettek között. Ha pl. egy magyar keverék előállító a terméket a magyarországi piacon is forgalomba kívánja hozni, úgy mind a VIII. melléklet szerinti, mind pedig a tevékenység bejelentési kötelezettségnek eleget kell tennie.
REACH hírek
Az ECHA újabb hét anyag engedélykötelessé tételére tesz javaslatot
Az ECHA hét anyag felvételét javasolja az Európai Bizottságnak a REACH rendelet engedélyköteles anyagokat tartalmazó XIV. mellékletébe. A melléklet anyaglistájára kerülést követően a cégeknek uniós engedélyt kell kérniük ezen anyagok további használatához.
Az ECHA (sorrendben immár tizedik) ajánlásában szereplő három, nagy mennyiségben gyártott és széles körben felhasznált ciklosziloxán (D4, D5 és D6) káros a környezetre és az emberi egészségre, és egyes felhasználásai már jelenleg is korlátozottak vagy korlátozásuk folyamatban van fogyasztási cikkekben és a legtöbb professzionális felhasználás tekintetében. A ciklosziloxánok felvételét az engedélyköteles anyagok közé prioritásként kezelték, mivel egyes felhasználásaikra, például az elektronikai ipari gyártásra nem vonatkoznak korlátozások.
A további anyagok közül a hidrogénezett terfenil, amelyet hőátadó folyadékként alkalmaznak, főleg ipari létesítményekben, valamint ragasztókban, tömítőanyagokban, bevonatokban, festékekben és műanyag árucikkekben is felhasználnak, káros a környezetre, a DCHP, a dinátrium-oktaborát és a TMA pedig az emberi egészséget károsítják.
A végső döntést, amelynek alapján ezeket a korábban már különös aggodalomra okot adóként azonosított anyagokat (Substances of Very High Concern – SVHC) felveszik az engedélyköteles anyagok közé, az Európai Bizottság hozza majd meg az EU tagállamaival és az Európai Parlamenttel együtt. Ezek a határozatok azokat a dátumokat is megjelölik, ameddig az érdekelt cégeknek az anyagok további használatának engedélyezéséhez kérelmet kell benyújtaniuk.
A REACH rendelet szerinti engedélyezés célja annak biztosítása, hogy a különös aggodalomra okot adó anyagok felhasználásából eredő kockázatokat megfelelően ellenőrizzék, és hogy fokozatosan kevésbé veszélyes anyagokkal vagy technológiákkal helyettesítsék azokat, amennyiben technikailag és gazdaságilag megvalósítható alternatívák állnak rendelkezésre.
További információ
Tizedik ajánlás [EN] [PDF]
Különös aggodalomra okot adó anyagok engedélyezésének jelöltlistája (Candidate list)
Az engedélyköteles anyagok listája
Forrás: ECHA
CLP hírek
2021. április 26-án megszűnik a PCN vezetett dossziékészítése
Az ECHA PCN bejelentési portálja jelenleg különböző módokon biztosítja az ipar számára (egyszerűsített, ún. vezetett dossziékészítés és adatkészlet alapú dossziékészítés), hogy a veszélyes keverékekre vonatkozó információkat elkészítse és benyújtsa a méregközpontok felé.
A PCN portálon 2021. április 26-tal azonban megszűnik a vezetett dossziékészítés és a továbbiakban csak az adatkészlet (dataset) nézet marad fent. Azon felhasználóknak, akik gyakran jelentenek be, érdemes tüzetesen megismerkedniük ezzel a felülettel a könnyebb átállás érdekében.
A váltás célja a PCN bejelentési felület átláthatóbbá, és ezáltal a bejelentés menetének gördülékenyebbé tétele. A bejelentés során először a keverék adatkészletét kell létrehozni, ez szolgál a dosszié alapjául. A lenyitható fülekkel könnyen és gyorsan elérhetőek a bejelentés pontjai, az adatok kitöltésének sorrendjét így a bejelentő döntheti el. Különböző munkakörnyezeteket (working context) hozhatunk létre, így a rendszer csak azon kitöltendő mezőket jeleníti meg, ami a konkrét bejelentéshez szükséges. Amennyiben a bejelenteni kívánt keverék MiM-et (keverékben lévő keverék) vagy egyéb speciális összetevőt tartalmaz (pl. helyettesítő összetevők csoportját vagy szabványos formulának megfelelő keveréket), ezen információkat egy külön munkakörnyezetben is meg lehet adni, és később összekapcsolni a bejelenteni kívánt keverék adatkészletével. Az összekapcsolt adatkészletek esetében bármelyikben változtatás történik, a módosított információk a többi adatkészletben is meg fognak jelenni.
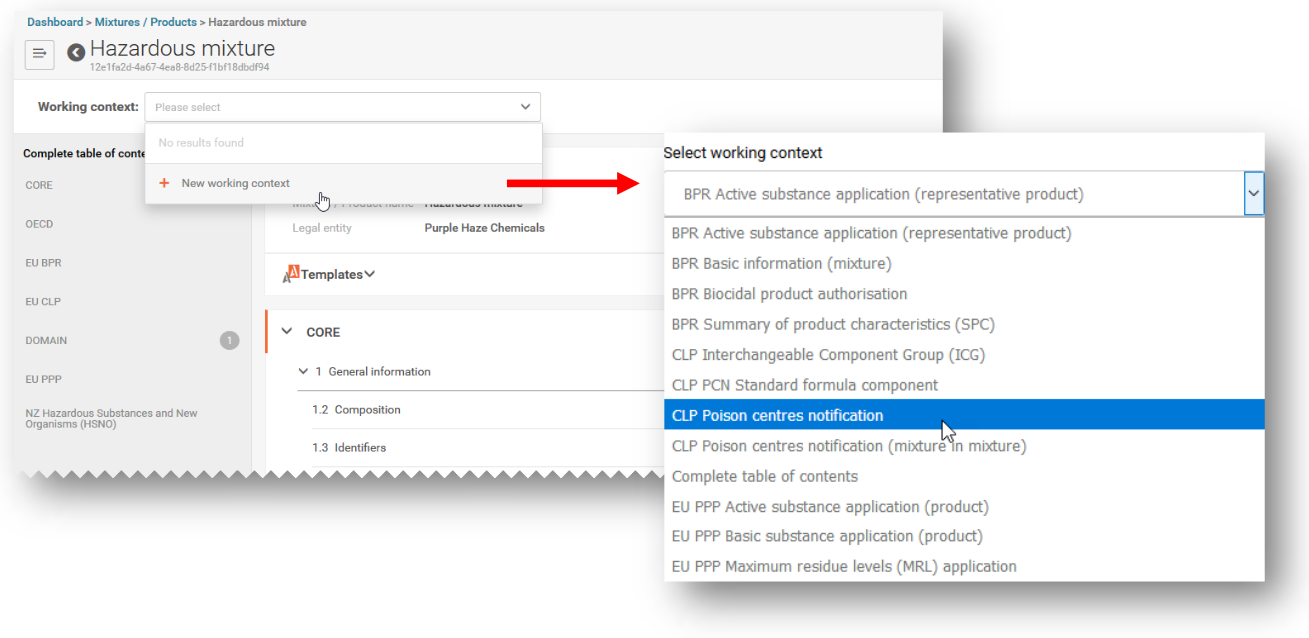
Az adatkészlet szerkeszthető: a bejelentő hozzáadhat, eltávolíthat vagy módosíthat keverékkel kapcsolatos adatokat. Ebből készül el a dosszié, melyet a tagállami méregközpontok felé küldenek, amely már nem módosítható.
Az adatkészlet nézet előnyei a vezetett dossziékészítéssel szemben:
- átláthatóbb menüpontok
- szükségtelen mezők mellőzése
- jobb felületeloszlás, így egyszerre több információ látható
- felkészíti a rendszert a csoportos bejelentés* lehetőségére
Az adatkészletek elkészíthetők az irányítópult „Keverékek” („Mixtures”) moduljában. Az irányítópulton található az „Anyagok” („Substances”) modul is, amelyben bármilyen anyag adatait tárolhatja, akár egyedileg elkészítve, akár beimportálva. Az „Árucikkek” („Articles”) modul csak a SCIP adatbázisba történő bejelentésekhez használható, amely információkat tartalmaz az árucikkekben található, aggodalomra okot adó anyagokról.
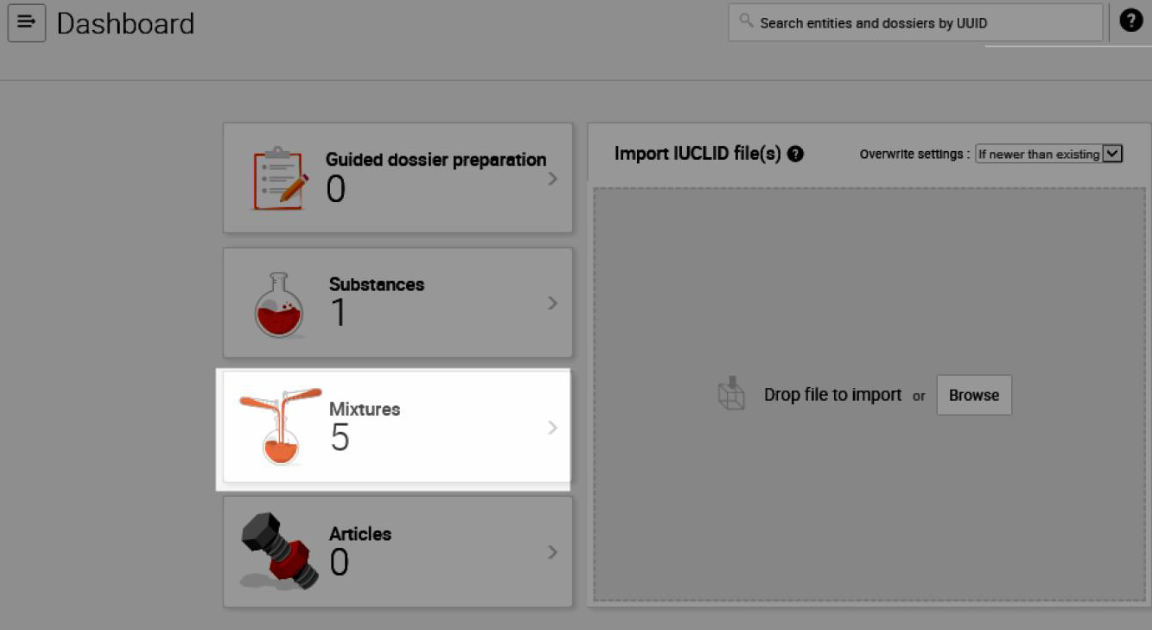
Segítséget nyújtanak a méregközponti bejelentés megtételéhez a Nemzeti Népegészségügyi Központ honlapján fellelhető ECHA videók, melyek magyar nyelvű felirattal vannak ellátva:
Az adatkészlettel történő bejelentésről szóló hivatalos segédlet „PCN: a practical guide” néven érhető el az alábbi weboldalon:
https://poisoncentres.echa.europa.eu/hu/echa-submission-portal
* Az összetételükben csak korlátozottan eltérő többféle keverékre vonatkozó információkat meg lehet adni ugyanabban a bejelentésben: ezt nevezik „csoportos bejelentésnek”. Eltérés lehetséges, mely kizárólag illatszert, illatanyagot érinthet, melyek együttes koncentrációja nem haladhatja meg az 5%-ot. A PCN bejelentés ezen funkciója várhatóan a 2021-es év második felében élesedik.
Az aeroszolos szóróadagolókban lévő keverékek osztályozása egészségi és környezeti veszélyek szempontjából
Az EU-tagállamok REACH- és CLP Kompetens Hatóságainak fő fórumán, a ’CARACAL’-on már hosszabb ideje napirenden szerepelt az aeroszol-termékek helyes veszélyességi besorolásának kérdésköre. A számos egyeztetés eredményeként született, harmonizált iránymutatás most az Európai Vegyianyag-ügynökség (ECHA) weboldalán elérhető, rendszeresen frissülő ’Kérdések és válaszok’ (Q&As) között mindenki számára könnyen hozzáférhetővé vált, rövid, tömör leírást adva az érintett vállalatok számára ebben a kérdésben, angol nyelven.
A fentiek alapján, amennyiben Magyarországon aeroszolos szóróadagolókkal ellátott terméket hoznak forgalomba, annak – az aeroszol termékekre vonatkozó 34/2014. (X. 30.) NGM rendelet mellett – meg kell felelnie a veszélyes anyagok és keverékek osztályozásáról, címkézéséről és csomagolásáról szóló 1272/2008/EK (CLP) rendelet, valamint a kémiai biztonságról szóló 2000. évi XXV. törvény (Kbtv.) előírásainak is. Ezzel összhangban, a termékben lévő keverékhez hozzáadott hajtóanyag vagy más gáz veszélyességi besorolása az alábbiak szerint játszik szerepet a termék (a keverék) osztályozásakor:
1) Ha a hozzáadott anyag a permetezéskor nem szabadul fel, nem vesszük figyelembe az aeroszoladagolóban lévő keverék osztályozásakor.
2) Ha a permetezéskor részben vagy teljesen felszabadul, de elkülönül a keverék összetevőitől, ugyancsak nem vesszük figyelembe a keverék osztályozásakor. Az elkülönülést a keverék többi összetevőjétől akkor feltételezzük, ha a hajtóanyag vagy más gáz nem cseppfolyós, vagy cseppfolyós, de gőznyomása (20°C-on) nagyobb vagy egyenlő, mint 10 kPa.
3) Ha a permetezéskor részben vagy teljesen felszabadul, azonban nem különül el a keverék többi összetevőjétől, ebben az esetben már figyelembe kell vennünk az aeroszoladagolóban lévő keverék osztályozásakor. Folyékony halmazállapotú hajtóanyag esetében tehát akkor, ha annak gőznyomása (20°C-on) 10 kPa alatti érték, valamint akkor, ha a gőznyomása 10 kPa feletti érték ugyan, de egyértelműen bizonyítható, hogy nem különül el a keverék többi összetevőjétől.
Az első és második esetben is fontos azonban, hogy ha maga a hajtóanyag vagy más gáz az emberi egészségre vagy a környezetre veszélyesnek minősül a CLP rendelet alapján, az aeroszoladagoló címkéjének ezt a veszélyességi osztályozást is tartalmaznia kell.
Biocid hírek
A biocid termékekben felhasznált hatóanyagok soron következő jóváhagyásai
A következő években három újabb hatóanyag kerül jóváhagyásra, melynek következtében a kizárólag e hatóanyagokat tartalmazó termékek uniós biocid rendelet szerinti „újra-engedélyezése” válik kötelezővé.
Egy hatóanyag jóváhagyása igen összetett, több tagállamot, nemzetközi szervezetet és bizonyos esetekben nyilvános konzultációt magában foglaló eljárás, melynek eredményeképpen meghatározásra kerülnek az adott hatóanyag felhasználhatóságának alapkövetelményei. A hatóanyag értékelése a kémiai meghatározáson túl kiterjed a hatóanyag biocidként történő felhasználásának emberi és állati egészségre gyakorolt hatásaira, illetve a célszervezettel szembeni kellő hatásosság eldöntésére. A feladat összetettségéből adódóan a jóváhagyási eljárás hosszadalmas és jelentős munkaterhet ró mind az értékelő hatóságra, mind a hatóanyag jóváhagyását támogató cégekre. A biocid szabályozás értelmében 2024 végére minden hatóanyag jóváhagyásának meg kell történnie.
Egy hatóanyag jóváhagyása nem jár azonnali következménnyel az adott hatóanyagot tartalmazó biocid termékekre, a jóváhagyásról szóló joganyag közzétételét közel másfél éves türelmi idő után kell csak megkezdeni az újra-engedélyezési eljárást. Az eljárás megkezdésének határideje a hatóanyag jóváhagyásáról szóló végrehajtási rendeletben szereplő „jóváhagyás dátuma”. Ezen hosszú időintervallum megtévesztő lehet, ugyanis a még nem jóváhagyott hatóanyagokat tartalmazó, úgynevezett átmeneti időszakos termékek engedélyezési folyamatához képest az újra-engedélyezési eljárás jelentősen szigorúbb feltételeket és bővebb adatkövetelményt támaszt, így a felkészülésre rendelkezésre álló egy-másfél éves türelmi idő meglehetősen szűkösnek bizonyulhat. Különösen igaz ez akkor, ha az újra-engedélyeztetés jogvesztő határidejére olyan vizsgálatok elvégzése válik szükségessé, melyek vizsgálati szakasza is meghaladja az említett türelmi időt. Fentiekre tekintettel az újra-engedélyezési eljárásra történő felkészülést érdemes időben elkezdeni.
A 2021. évben már forgalomban lévő hatóanyag jóváhagyására nem kerül sor. A soron következő, a mai napig közzétett jóváhagyási dátumok:
|
Hatóanyag |
EC-szám |
CAS-szám |
Felvételi határozat |
Terméktípus |
Jóváhagyás napja |
|
Formaldehid |
200-001-8 |
50-00-0 |
2, 3 |
2022. február 1. |
|
|
Ikaridin |
423-210-8 |
119515-38-7 |
19 |
2022. február 1. |
|
|
Karbendazim |
234-232-0 |
10605-21-7 |
7, 10 |
2022. február 1. |
|
|
Perecetsav (PAA) és a peroxioktán-sav (POOA) reakciótömege |
201-186-8 450-280-7 |
79-21-0 33734-57-5 |
2, 3, 4 |
2022. április 1. |
|
|
Hipoklóros-savból felszabaduló aktív klór |
232-232-5 |
7790-92-3 |
2, 3, 4, 5 |
2022. július 1. |
|
|
Nátrium-kloridból elektrolízissel előállított aktív klór |
231-598-3 |
7647-14-5 |
2 |
2022. július 1. |
Megjegyzendő, hogy a Hipoklórossavból felszabaduló aktív klór és a Nátrium-kloridból elektrolízissel előállított aktív klór hatóanyagok 1. terméktípusban történő jóváhagyási dátuma 2021. július 1., azonban ezen hatóanyagok a szabályozás tekintetében úgynevezett „új hatóanyagnak” minősülnek, így ilyen hatóanyagú termékek a jóváhagyás dátuma előtt nem lehetnek forgalomban az Unió területén.
Kéztisztító vagy kézfertőtlenítő? Mi nem szerepelhet egy címkén, ha a termék „csak” kéztisztító?
A kéztisztító, illetve kézfertőtlentő termékek esetében gyakran igen nehéz eldönteni, hogy kozmetikai termékről, biocid termékről (azon belül is fertőtlenítőszerről) vagy esetleg mindkettőről van szó. Ennek eldöntésében segít egy, az Európai Bizottság által kiadott, alábbiakban összefoglalt, a kozmetikai termékekre vonatkozó műszaki dokumentáció.
A koronavírus (COVID-19) terjedésének csökkentése érdekében az Európiai Unióban számos intézkedés született, ilyen például a szigorúbb higiéniai gyakorlatok alkalmazása is. A koronavírus (COVID-19) terjedése elleni megelőző intézkedésként az Európai Betegségmegelőzési és Járványvédelmi Központ a következőt ajánlja: „Bármilyen körülmények között ajánlott a legalább 20 másodpercig tartó, szappannal és vízzel való kézmosás, vagy a kéz alkoholos oldattal, géllel vagy törlőkendővel történő tisztítása”.
A különböző higiéniai gyakorlatok ajánlása miatt jelentősen megnőtt a kereslet a kéztisztító és kézfertőtlenítő gélek, törlőkendők illetve más nem leöblítendő termékek használata iránt. A nagyobb kereslet kielégítése érdekében számos gazdasági szereplő hajt végre vagy mérlegel olyan beruházásokat, amelyek segítségével a termelési lánc átállítható a kéztisztítók és kézfertőtlenítők gyártására, illetve amelyek révén növelhető az ilyen termékek gyártása.
Nagyon fontos azonban figyelemmel lenni arra, hogy a kéztisztítók és kézfertőtlenítők merőben különböző jogi keretek hatálya alá tartoznak, nevezetesen vagy a kozmetikai termékekről szóló rendelet vagy a biocid termékekről szóló rendelet hatálya alá. Ennek függvényében eltérő feltételeknek kell megfelelniük. Az, hogy egy adott termék mely termékkörbe tartozik az számos tényezőtől (például a termékre vonatkozó állításoktól, a termék összetételétől és rendeltetésétől) függ.
A kozmetikai termékekről szóló rendelet alapján:
„kozmetikai termék: minden olyan anyag vagy keverék, amely azt a célt szolgálja, hogy az emberi test különböző külső részeivel (hámréteg, haj és testszőrzet, körmök, ajkak és külső nemi szervek) vagy a fogakkal és a szájüreg nyálkahártyájával érintkezésbe kerüljön, kizárólag vagy elsősorban azok tisztítása, illatosítása, kinézetük megváltoztatása, védelme, megfelelő állapotban tartása céljából, vagy a testszag megszüntetése érdekében”
A biocid termékekről szóló rendelet alapján:
„biocid termék: bármely olyan, egy vagy több hatóanyagból álló, egy vagy több hatóanyagot tartalmazó vagy egy vagy több hatóanyagot keletkeztető anyag vagy keverék a felhasználóhoz jutó kiszerelésben, amelynek rendeltetése, hogy károsító szervezeteket a tisztán fizikai vagy mechanikai ráhatáson kívüli bármely módon elpusztítson, elriasszon, ártalmatlanná tegyen, hatásuk kifejtésében megakadályozzon vagy azokkal szemben más gátló hatást fejtsen ki”
Fentiek tekintetében, míg a szappan alapvetően a kozmetikai termékek közé tartozik, más termékek, például az alkoholalapú oldatok, gélek, kéztisztítók és -fertőtlenítők stb. esetében további pontosításra lehet szükség.
Az alábbi állítások azt sugallják, hogy egy kéztisztító gél főként biocid funkciót tölt be, így ezek a kijelentések megtévesztőek a kozmetikumokon, és feltételezhetően az adott termék a biocid termékekről szóló rendelet hatálya alá tartozik. Megjegyzendő, hogy a felsorolt példák mindegyike csak szemléltető jellegű.
A nem leöblítendő hidroalkoholos kéztisztító gél típusú kozmetikai termékeken nem használható címkeelemek:
Állítások (és azok változatai):
- antibakteriális, antimikrobiális, antivirális, vírusölő, gombaölő (és ezek bővítménnyel együtt használt változatai, mint például „vírusellenes tulajdonságok”, „antibakteriális összetevők”, „bakteriális növekedés megelőzése”);
- fertőtlenítő, fertőtlenítés;
- fertőtlenítő szer;
- a baktériumok/vírusok/mikrobák X %-át elpusztítja;
- sterilizáló;
- az Egészségügyi Világszervezet (WHO) által javasolt összetétel;
- COVID19 elleni, koronavírus elleni, SARS elleni.
Hivatkozások vagy utalások a következőkre:
- fertőzés, világjárvány, betegségek;
- COVID19, koronavírus, SARS-CoV-2;
- mikroorganizmusok, baktériumok, vírusok, kórokozók, csírák, gombák;
- fertőtlenítés;
- gyógyászati felhasználás;
- a termék százalékos alkoholtartalma;
- higiénikus kéz.
Képek vagy grafikus elemek:
- (korona)vírus, baktériumok, mikrobák;
- (vörös) kereszt (orvosi konnotáció felmerülése esetén);
- védőréteg (a mikroorganizmusok elleni védelem feltüntetésekor);
- STOP jelzés (egy betegség, fertőzés vagy mikrobák terjedésének megelőzése/kontrollálása esetén);
- kórházra, gyógyszertárra, betegszállító autóra, elsősegélynyújtásra stb. vonatkozó jelzések;
- CLP (azaz veszélyességre utaló) piktogramok.
A műszaki dokumentáció minden tagállami nyelven az alábbi, az Európai Bizottság honlapjára mutató hivatkozáson érhető el:
https://ec.europa.eu/docsroom/documents/44913
Kapcsolat
Cím: 1097 Budapest, Albert Flórián út 2-6.
Telefon: 06-1-476-1195
E-mail: Ez az e-mail-cím a szpemrobotok elleni védelem alatt áll. Megtekintéséhez engedélyeznie kell a JavaScript használatát.
Honlap: https://www.nnk.gov.hu/index.php/kemiai-biztonsagi-es-kompetens-hatosagi-fo/kbkhf-kezdolapja