Nyilvános konzultációk
|
REACH rendelet |
Korlátozási javaslatok |
A megadott linkre kattintva megnyíló oldal táblázatának utolsó oszlopában látható ’Details’, majd a ’Give Comments’ feliratra kattintva tehető észrevétel.
|
Határidő: november 14.
Határidő: december 20.
Határidő: 2023. március 22.
|
|
Határidő: november 18.
Határidő: december 16.
|
|||
|
CLP rendelet |
Harmonizált osztályozás és címkézés (CLH) |
REACH
Összefoglaló az Európai Vegyianyag-ügynökség díszítő krómozással foglalkozó konferenciájáról
Dr. Schuchtár Endre – az Európai Vegyianyag-ügynökség Társadalmi és Gazdasági Elemző Bizottságának magyar tagja
2022. október 10-én, 350 szakértő részvételével került megrendezésre egy online konferencia, amely rávilágított a háromvegyértékű krómmal történő helyettesítés megoldhatóságára, emellett felhívta a figyelmet ennek a jövőbeli alkalmazhatósági problémáira is.
A hatvegyértékű, CMR (rákkeltő, mutagén és reprotoxikus) tulajdonságokkal rendelkező króm (Cr(VI)) felhasználása 2017 óta az EU-ban a vegyi anyagok regisztrálásáról, értékeléséről, engedélyezéséről és korlátozásáról szóló REACH jogszabály (az Európai Parlament és a Tanács 2006. december 18-án elfogadott 1907/2006/EK rendelete: Registration, Evaluation, Authorisation and Restriction of Chemicals) által engedélyhez kötött, és díszítő krómozásban történő alkalmazása egyre több adminisztratív akadályba ütközik. Alternatívaként háromvegyértékű változata mutatkozik, és ezt ajánlják megoldásként az engedélykérelmekben az Európai Vegyianyag-ügynökség (ECHA) engedélyezési eljárásaiban résztvevő társadalmi szervezetek is.
Az Európai Bizottság (COM) a „Green Deal” jegyében hozta meg szigorításait, amely a REACH engedélyezési eljárását kiegészítette tavaly a SAGA (Suitable Alternative Generally Available – általánosan elérhető megfelelő helyettesítő) értékeléssel. A kérelmezőnek ebben azt kell a Cr(VI) további alkalmazásához részleteznie, hogy jelenleg miért nem tudja helyettesíteni, és mikor válik legkorábban képessé a helyettesítésre. A SEAC-nak véleményezési eljárásában tekintettel kell lennie a részben COM által finanszírozott társadalmi szervezetekre, amelyek az azonnali helyettesítést javasolják, és azon az állásponton van, hogy a technikailag és gazdaságilag megfelelő kérelmek elfogadhatók, azonban rövidebb időszakot javasolva, mint amit a Cr(VI) felhasználó cég vagy beszállítója kér a helyettesítésig.
A konferencia szakelőadói végigvették a Cr(III) felhasználásával dekoratív felület kialakítását eredményező eljárás részleteinek bemutatását; az alapanyag beszerzésétől a megvalósítás technológiáján át a végtermék tulajdonságainak jellemzéséig. Ezen összefoglalónak nem célja a technikai részletekbe menő információ adása, az azonban igen, hogy felhívja a figyelmet e krómozási eljárásban a bórsav (H3BO3) jelenlétének szükségességére, amely nélkül a galvanizáció útján leválasztott krómfelület csak változó vastagságban (szín és korróziós probléma) és túl lassan (gazdasági kérdés) alakul ki. Az eljárás során a levegőbe kerülő borátok ellen a dolgozók munkahelyi védelme megoldható, de a szennyvízből történő kiszűrésük jelenleg még nem. Bár a bór reprotoxikus hatása ismert, még nem került azonosításra különös aggodalomra okot adó anyagként, így ma, jogi értelemben a Cr(III) tökéletes helyettesítő anyag. A közeljövő mindamellett már hozhat változást e tekintetben.
A konferencia témájával kapcsolatban, 15 éves SEAC tagságom alapján, a következő személyes tapasztalataimat oszthatom meg. A REACH rendelet megfelelő jogi keretet adott egy ambiciózus, a veszélyes anyagok kockázatos felhasználásának megszüntetését célzó terv megvalósításához az EU-ban. Ennek keretében sok anyag (pl. nehézfémek) és felhasználás korlátozása történt meg az ECHA tudományos testületei (RAC, SEAC) véleménye alapján, az EU Bizottság döntésével. A REACH jogszabály lehetővé teszi a korrekciót; ha a tiltás olyan felhasználást érint, amelynek esetében a kockázatok mértékénél sokkal jelentősebb gazdasági érdekek sérülnének a megfelelő alternatíva hiányában, az engedélyezési eljárás kínál megoldást. Ez a helyzet áll fenn a krómozással kapcsolatban, amely az elmúlt 5 év engedélyezési kérelmeit uralta. A díszítő krómozás kérelmeinek nyilvános konzultációi során a társadalmi szervezetek azt a véleményt képviselték, hogy a biztonságos helyettesítés már megoldott (ill. csak a cégek profit érdekeltsége miatt kerül sor az engedély megkérésére). Ennek mondott ellent ez a szakkonferencia, amely szerint a kézenfekvő helyettesítés (vagyis a Cr(VI) helyettesítése Cr(III)-mal) is kockázatot rejt magában, és ennek fényében továbbra is indokoltak lehetnek a vonatkozó engedélyezések, valamint rámutatott a felgyorsított és erőltetett „zöldítés” veszélyeire.
További információk:
A workshopon bemutatott előadások és az összefoglaló elérhető az esemény weboldalán
CLP
A CLP rendelet hozzáigazítása a műszaki és tudományos fejlődéshez
2022. december 17-től már kötelezően alkalmazandó a Bizottság (EU) 2021/849 felhatalmazáson alapuló rendelete, amely az anyagok és keverékek osztályozásáról, címkézéséről és csomagolásáról szóló 1272/2008/EK rendelet (CLP rendelet) VI. mellékletének 3. részét módosítja, a műszaki és tudományos fejlődéshez való hozzáigazítás céljából (ún. 17. ATP). Ez azt jelenti, hogy a veszélyes anyagok harmonizált osztályozási és címkézési jegyzéke új bejegyzésekkel egészül ki, valamint módosulnak már meglévő bejegyzések, és törlésre kerül egy bejegyzés.
Az újabb bejegyzések közé tartozik például a háztartási és öko-tisztítószerekben is széles körben alkalmazott citromsav (EK-szám: 201-069-1) (harmonizált osztályozása) is, amelyet a fentiek alapján a következő veszélyességi osztályokba és kategóriákba kell kötelezően besorolni: Szemirritáció, 2. kategória, H319 és Célszervi toxicitás, egyszeri expozíció, 3. kategória, H335, az anyag szem- és légúti irritációt okozó hatására tekintettel.
A rendeletnek való megfelelés a szállítói lánc minden tagját érinti, így a gyártóknak, importőröknek, továbbfelhasználóknak és forgalmazóknak egyaránt gondoskodniuk kell arról, hogy az érintett anyagok és keverékek címkézése és csomagolása megfeleljen az új előírásoknak a forgalomba hozatalt megelőzően, valamint eleget tegyenek a veszélyes keverék-bejelentési kötelezettségüknek, amennyiben az az új harmonizált osztályozások alkalmazása miatt szükségszerűvé válik.
További információk:
A Bizottság (EU) 2021/849 felhatalmazáson alapuló rendelete
Ökovegyszerek - Magunkat is védjük, ne csak a környezetet!
Az utóbbi évtizedekben egyre nagyobb hangsúlyt kap a környezetvédelem, és az ipari mértékű környezetszennyezés csökkentésén túl mindennapi életünkben is több helyen tetten érhető a környezetre káros hatások csökkentésére való törekvés, gondoljunk csak a szelektív hulladékgyűjtésre vagy az energiatakarékos háztartási berendezésekre.
A környezet megóvása érdekében tett törekvések hatására egyre többször találkozhatunk ún. ökocímkével rendelkező termékekkel. Ezekre a termékekre általánosságban az a jellemző, hogy előállításuk, felhasználásuk és újrahasznosításuk a lehető legkisebb környezeti terhelés mellett valósul meg.

Az Európai Unióban 1992-ben határozták meg először az ökocímkék odaítélésére vonatkozó kritériumrendszert, amely mostani formáját 2010-ben nyerte el. Számos termékkategória kaphatja meg ezt a címkét, mint pl. elektronikai berendezések, vegyiáruk (pl. mosó- és tisztítószerek), ruházati termékek. Az egyes terméktípusokhoz külön kritériumrendszer került meghatározásra, de minden esetben elmondható, hogy nem ítélhető oda a címke, amennyiben a termék az anyagok és keverékek osztályozásáról, címkézéséről és csomagolásáról szóló 1272/2008/EK rendelet (CLP rendelet) értelmében mérgező, környezetre veszélyes, rákkeltő, mutagén vagy a szaporodóképességre káros besorolással rendelkező anyagot vagy keveréket, illetve a vegyi anyagok regisztrálásáról, értékeléséről, engedélyezéséről és korlátozásáról szóló rendelet szerinti engedélyköteles anyagot tartalmaz.
A mosó- és tisztítószerek, és általában a vegyiáruk esetében - a szigorú feltételrendszer ellenére - sem szabad figyelmen kívül hagyni, hogy bár ezek a termékek a környezetre a lehető legkisebb veszélyt jelentik és súlyos egészségkárosodást nem okozhatnak, azonban hatóanyagaik miatt az emberi egészségre mégis károsak lehetnek, pl. bőrirritáló vagy allergiás reakciót kiváltó hatásuk miatt.
A CLP rendelet uniós szinten szabályozza azt, hogy a vegyi anyagot tartalmazó termékek címkéjén milyen információkat kell feltüntetni annak érdekében, hogy a vásárló pontos tájékoztatást kapjon a termék veszélyeiről, a biztonságos tárolásról és kezelésről, illetve az óvintézkedésekről. Az ún. piktogram a leginkább figyelemfelkeltő elem a címkén. Az egyes piktogramok különböző veszélyességi kategóriákhoz tartoznak, pl. a felkiáltójel jelzi a bőr- és szemirritáló, allergiás bőrreakciót kiváltó, illetve lenyelve, belélegezve vagy bőrrel érintkezve ártalmas anyagokat. Ezek a kategóriák az alábbi ábrán a piktogram mellett kerültek feltüntetésre. Az ökotermékeken a bekeretezett piktogramok fordulhatnak elő.
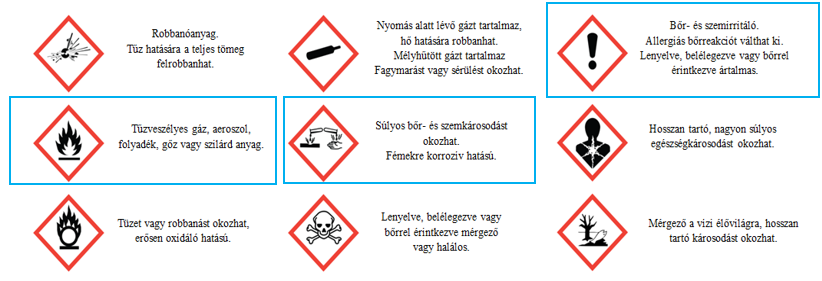
Akár öko-, akár hagyományos terméket vásárol, használat előtt mindig olvassa el a címkét és tartsa be az azon feltüntetett utasításokat, így védve nem csak a környezetet, hanem saját és családtagjai egészségét is.
Felülvizsgálatra került az átmeneti időszak utáni UFI kód-feltüntetési kötelezettség értelmezése
Az Európai Vegyianyag-ügynökség (ECHA) frissítette az egyedi formulaazonosító (UFI) címkén való feltüntetésére vonatkozó határidővel kapcsolatos, 1727-es számú kérdés-válasz párt. A kérdés arra vonatkozik, hogy maradhatnak-e a polcokon az 1272/2008/EK (CLP) rendelet VIII. mellékletének hatálya alá tartozó, már 2025. január 1-je előtt forgalomba hozott veszélyes keverékek ezen időpontot követően, további szállítás céljából, UFI feltüntetése nélkül.
A felülvizsgált válasz úgy fogalmaz, hogy ezek a már a polcokon lévő keverékek akkor forgalmazhatók tovább, ha a kötelezettek (a továbbfelhasználók és importőrök) már benyújtották azon nemzeti követelményeknek megfelelő információkat, amelyekre vonatkozik a 2025. január 1-jéig tartó átmeneti időszak, és nem hoztak létre UFI-t a keverék címkézésekor.
Az a kötelezett, aki tehát a megfelelő határidők előtt olyan tagállami követelmények alapján tett bejelentést, amelyek nem felelnek meg a VIII. melléklet követelményeinek, 2025-ig még élhet az átmeneti időszak nyújtotta előnyökkel, és legkésőbb 2025. január 1-jéig még nem kell feltüntetnie az UFI-t a címkén.
Az a keverék, amelyre vonatkozóan a kötelezett 2025. január 1-jéig még élvezi az átmeneti időszak előnyeit, akkor is megfelel a CLP rendeletnek, ha a terméket azt követően is UFI nélkül forgalmazzák. Ennek oka, hogy a CLP rendelet 25. cikkének (7) bekezdése szerint a keverékeket csak akkor kell UFI-val ellátni, ha a VIII. melléklet szerint a benyújtó egyedi formulaazonosítót hoz létre. Ha 2025. január 1-je előtt a kötelezett nem hozott létre UFI-t a keverék címkézésekor, a keverék akkor is megfelel a CLP rendeletnek, ha azt később a címkén feltüntetett UFI nélkül forgalmazzák.
Azok a kiskereskedők (forgalmazók), akik olyan veszélyes keveréket kaptak, amelyre vonatkozik az átmeneti időszak, továbbra is forgalomba hozhatják azt a címkén feltüntetett UFI nélkül, mivel a kötelezetteknek addig nem kellett UFI-t létrehozniuk. Megjegyzendő, hogy azokban az esetekben, amikor a forgalmazók tevékenysége a CLP rendelet 4. cikkének (10) bekezdése értelmében bejelentési kötelezettséggel jár, a keverék ezzel összhangban nem hozható forgalomba a címkén szereplő UFI feltüntetése nélkül.
A kötelezetteknek csak attól az időponttól kezdve kell létrehoznia az UFI-t, amikor már nem vonatkozik rájuk az átmeneti időszak. Ez szükségessé teheti a már raktáraikban és polcaikon lévő termékek újracímkézését, akár olyan módon is, hogy az UFI-t a meglévő címkéken matricák segítségével tüntetik fel (az UFI címkén való elhelyezésével kapcsolatos további információkért lásd az ECHA-nak a CLP rendelet szerinti címkézésről és csomagolásról szóló útmutatóját). Ez a lehetőség elkerülhetővé teszi a címkék újranyomtatását és teljes cseréjét.
További információk:
Az ECHA vonatkozó Kérdések és válaszok weboldala
Az ECHA CLP rendeletre vonatkozó útmutatóinak weboldala
Forrás: ECHA
Bejelentés
A PCN bejelentéshez összeállított, adatközlésre javasolt mintatáblázat használata
Az NNK által összeállított, adatközlésre javasolt mintatáblázat első blokkja (A1-B8 mezők) tartalmazza a számviteli bizonylat kiállításához szükséges adatokat, mint: a cég neve, címe, adószáma (külföldi befizető esetén országkóddal kell megadni, valamint a számsor elején szereplő „0”-ákat is fel kell tüntetni), e-mail címe (amelyre a befizetést igazoló dokumentumot kérik megküldeni), továbbá külföldi befizető esetén a SWIFT és IBAN kódokat.
A táblázat használata nagymértékben elősegíti a befizetések beazonosítását, ezzel elősegítve a gördülékeny, hatékony ügyintézést.
A 3 bejelentés-típus esetén a táblázat kitöltésével kapcsolatos tudnivalók:
Kezdeti/új bejelentés esetén:
Az első oszlopban a kezdeti benyújtási számot kell beírni, a második oszlopban a bejelentés típusaként a „Kezdeti” típust kell kiválasztani a lenyíló listából, a harmadik oszlopot üresen kell hagyni, a negyedik oszlopban a termék nevét kell beírni és végül az ötödik oszlopban a benyújtás dátumát kell megadni.
Változás bejelentés esetén:
Amennyiben naprakésszé tették (frissítették) a bejelentést (nem ide értendő az összetételt érintő jelentős változás bejelentés esete), úgy a változás bejelentéshez (update) tartozó benyújtási számot kell megadni az első oszlopban, a második oszlopban a bejelentés típusaként a „Változás”-t kell kiválasztani a lenyíló listából, a harmadik oszlopban a bejelentés kezdeti benyújtási számát kell feltüntetni, a negyedik oszlopban a termék nevét és végül az ötödik oszlopban a változás bejelentés benyújtásának dátumát kell beírni.
Ha egy esetleges frissítés a termék magyar piacra történő kiterjesztését (is) jelenti, akkor a változás bejelentés a magyarországi bejelentettségre nézve új, kezdeti bejelentésnek fog minősülni, melynek díja 16 000 Ft/bejelentés.
Összetételt érintő jelentős változás bejelentés esetén:
Az első oszlopban az összetételt érintő jelentős változás bejelentéshez tartozó benyújtási számot kell beírni, a második oszlopban a bejelentés típusaként az „Összetételt érintő jelentős változás”-t kell kiválasztani a lenyíló listából, a harmadik oszlopban a bejelentés kezdeti benyújtási számát kell feltüntetni, a negyedik oszlopban a termék nevét és végül az ötödik oszlopban az összetételt érintő jelentős változás bejelentés benyújtási dátumát kell beírni.
Előfordul olyan eset is, hogy a magyarországi piackiterjesztést és az összetételt érintő jelentős változás bejelentést egyidejűleg teszi meg a bejelentő. Ebben az esetben is fennáll, hogy a veszélyes keverék a magyarországi bejelentettségre nézve új, kezdeti bejelentésnek fog minősülni, így annak a díja ugyancsak 16 000 Ft/bejelentés.
A táblázat egyes cellái pirosra színeződnek, amennyiben egy adott mezőben bizonyos adat megadása mindenképpen szükséges.
A mintatáblázatok magyar és angol nyelvű verziói:
PCN adatszolgáltatás_Cégnév_Dátum
Biocidok
Frissült a biocid termékek engedélyezésével kapcsolatos tájékoztatás
A biocid termékek átmeneti időszakos és uniós rendelet szerinti engedélyezésével kapcsolatos tájékoztatás, illetve a vonatkozó segédletek (beleértve az ÁNTSZ honlapon elérhető tartalmakat is) felülvizsgálatra és naprakész formában kihelyezésre kerültek a Nemzeti Népegészségügy Központ honlapján. A gördülékeny engedélyezés és a gyors információszolgáltatás érdekében tisztelettel kérjük, hogy az engedélyezési kérelmek benyújtása, illetve a Biocid Helpdesk számára küldött megkeresések feladása előtt a https://www.nnk.gov.hu/index.php/kemiai-biztonsagi-es-kompetens-hatosagi-fo/biocid elérhetőségű oldalon tájékozódni szíveskedjék. A honlapon közzétett információkon túlmutató megkeresése esetén továbbra is szívesen állunk rendelkezésére az eddigi elérhetőségeken.
A Biocid termékekkel foglalkozó bizottság és a hatóanyag-terméktípus kombináció jóváhagyásának menete
Az ECHA biocid termékekkel foglalkozó bizottsága (BPC) megtartotta soron következő, 44. ülését. A bizottság feladatait és a hatóanyag-terméktípus kombinációk jóváhagyásának menetét a 2022/2. számú hírlevélben foglaltuk össze.
A 44. BPC ülésen tárgyalt napirendi pontok:
Hatóanyag-terméktípus kombinációk
|
Hatóanyag neve |
CAS szám |
Terméktípus |
Vélemény |
|
Oxigénből generált ózon |
n.a. |
2, 4, 5, 11 |
jóváhagyásra javasolt |
|
Mecetrónium metil szulfát |
3006-10-8 |
1 |
jóváhagyás megtagadása javasolt |
|
Kén-dioxid égetéssel generálva |
7446-09-5 |
4 |
jóváhagyásra javasolt |
| Nátrium-metabiszulfátból felszabaduló kén-dioxid | prekurzor: 7681-57-4 | 9 | jóváhagyásra javasolt |
A közzétett vélemények elérhetősége:
https://echa.europa.eu/regulations/biocidal-products-regulation/approval-of-active-substances/bpc-opinions-on-active-substance-approval
Uniós szintű termékengedélyezés:
Öt termékcsalád engedélyezési dokumentációjának véleményezése.
A közzétett vélemények elérhetősége:
https://echa.europa.eu/opinions-on-union-authorisation/bpc
Egyéb tárgyalt kérdések:
A BPR 15. cikke alapján a Bizottság felkérte a BPC-t a jód-PVP jód hatóanyag endokrin diszruptor tulajdonságának értékelésére.
A véralvadásgátló rágcsálóirtó hatóanyagok estében összehasonlító értékelő tanulmány készítése a lehetséges alternatív kémiai valamint nem-kémiai rágcsálóirtók felmérése vonatkozásában, társadalmi-gazdasági felmérés ismertetése.
Kapcsolat
Cím: 1097 Budapest, Albert Flórián út 2-6.
Telefon: 06-1-476-1195
E-mail: Ez az e-mail-cím a szpemrobotok elleni védelem alatt áll. Megtekintéséhez engedélyeznie kell a JavaScript használatát.
Honlap: https://www.nnk.gov.hu/index.php/kemiai-biztonsagi-es-kompetens-hatosagi-fo/kbkhf-kezdolapja